Миотокс
- (Артикул: 3445)
- Код товара: 3445
- Доступность: На складе
- Чтобы увидеть цену необходимо зарегистрироваться
Данные о ценах и наличии товаров находятся в режиме тестирования. Пожалуйста, уточняйте точную стоимость и наличие товаров в магазинах. Они могут отличаться от опубликованных на сайте.
Первая в мире жидкая стабильная форма ботулотоксина!
Ботулинический токсин типа А - гемагглютинин комплекс
Регистрационный номер: ЛП-005821.Торговое наименование: Миотокс®.
Международное непатентованное или группировочное наименование: Ботулинический токсин типа А – гемагглютинин комплекс.
Лекарственная форма: раствор для внутримышечного введения.
Состав на 1 флакон:
| Наименование компонента | Количество |
| Действующее вещество: | |
| Ботулинический токсин типа А – гемагглютинин комплекс | 100 ЕД |
| Вспомогательные вещества: | |
| Альбумин человека | 0,5 мг |
| Натрия хлорид | 9,0 мг |
| Вода для инъекций | до 1 мл |
Описание: Прозрачная или слабо опалесцирующая жидкость от бесцветного до светло-желтого цвета.
Фармакотерапевтическая группа: Миорелаксант периферического действия.
Код АТХ: М03АХ01.
Фармакологические свойства
Фармакодинамика
Молекула ботулинического токсина типа А состоит из двух цепей: тяжелой (с молекулярной массой 100 000 Да) и легкой (с молекулярной массой 50 000 Да), соединенных дисульфидной связью.
Тяжелая цепь обладает высоким сродством к специфическим рецепторам, локализованным на поверхности нейронов-мишеней. Легкая цепь характеризуется Zn2+ - зависимой протеазной активностью. Она специфична в отношении цитоплазматических участков синаптосомально связанного протеина с молекулярной массой 25 000 Да (SNAP-25), принимающего участие в процессах экзоцитоза.
Первая стадия действия ботулинического токсина типа А заключается в специфическом связывании молекулы с пресинаптической мембраной.
Вторая стадия – проникновение связанного токсина в цитоплазму нейронов путем эндоцитоза. Внутри клетки легкая цепь проявляет Zn2+ -зависимую протеазную активность, избирательно разрушая белок SNAP-25, что на третьей стадии приводит к блокаде высвобождения ацетилхолина из пресинаптических окончаний холинергических нейронов.
Конечным результатом является продолжительная хемоденервация.
При внутримышечной инъекции ботулинического токсина типа А развиваются 2 эффекта: прямое ингибирование экстрафузальных мышечных волокон посредством ингибирования альфа-мотонейронов на уровне нервно-мышечного синапса и ингибирование активности мышечных веретен посредством ингибирования гамма-мотонейронного холинергического синапса на интрафузальном волокне. Снижение гамма-активности ведет к расслаблению интрафузальных волокон мышечного веретена и уменьшает активность 1а-афферентов. Это приводит к снижению активности как мышечных рецепторов растяжения, так и эфферентной активности альфа- и гамма-мотонейронов. Клинически это проявляется в выраженном расслаблении инъецированных мышц и в значительном уменьшении боли в них. Наряду с процессом денервации в этих мышцах, идет процесс реиннервации путем появления боковых отростков нервных окончаний, что приводит к частичному восстановлению мышечных сокращений через 4-6 месяцев после инъекции.
Клинически отмечается выраженное расслабление мышц, в которые была произведена инъекция. В денервированных мышцах происходит процесс реиннервации за счет формирования латеральных отростков нервных окончаний через 12 недель после инъекции, что приводит к восстановлению мышечных сокращений. Однако, отростки эффективны частично и впоследствии регрессируют, в то время как первичная нейромышечная передача активируется.
Фармакокинетика
Фармакологический эффект препарата развивается в месте инъекции. Доказано, что пресинаптический захват и ретроградный аксональный транспорт препарата из места введения незначителен.
В терапевтических дозах препарат не проникает через гематоэнцефалический барьер и не вызывает существенных системных эффектов. Выводится почками в виде нетоксичных метаболитов.
Антитела к ботулиническому токсину типа А могут формироваться после повторных инъекций в 1-5 % случаев. Продукции антител способствует введение больших доз препарата, а также повторное введение в малых дозах через короткие промежутки времени (менее 14 дней). При формировании антител к ботулиническому токсину типа А эффект от его дальнейшего применения может быть сниженным.
Показания к применению
Препарат Миотокс® применяют у пациентов при следующих заболеваниях:
У взрослых:
– Блефароспазм;
– Цервикальная дистония (спастическая кривошея);
– Временная коррекция внешнего вида мимических морщин верхней трети лица (межбровных, лобных морщин и периорбитальных морщин) у взрослых.
У детей старше от двух лет и старше:
– Фокальная спастичность, ассоциированная с динамической деформации стопы по типу «конская стопа» вследствие спастичности у пациентов с детским церебральным параличом.
Противопоказания
Общие:
– Гиперчувствительность в анамнезе к любому компоненту препарата;
– Воспалительный процесс в месте предполагаемой инъекции (инъекций);
– Острая фаза инфекционных заболеваний;
– Беременность и период грудного вскармливания.
Дополнительные противопоказания при применении при блефароспазме и коррекции морщин верхней трети лица:
– Выраженный гравитационный птоз тканей лица;
– Выраженные «грыжи» в области верхних и нижних век.
– Период менее 3 месяцев после перенесенной хирургической операции на лице.
Дополнительные противопоказания при коррекции морщин верхней трети лица:
– Миастения гравис или синдром Ламберта-Итона.
С осторожностью
Препарат применяют с осторожностью:
– У пожилых пациентов с отягощенным анамнезом и сопутствующей лекарственной терапией;
– У пациентов, имеющих дисфагию и аспирацию в анамнезе;
– У детей с тяжелыми неврологическими нарушениями, дисфагией, заболеванием легких или недавно перенесших аспирационную пневмонию;
– У пациентов с патологическими изменениями роговицы (при проведении инъекции в области лица);
– У пациентов с экхимозами в месте введения препарата;
– У пациентов с нарушениями свертываемости крови и в случае сопутствующей терапии антикоагулянтами;
– В случае выраженной слабости или атрофии в мышце, в которую планируется вводить препарат;
– У пациентов с периферической моторной нейропатией (например, при амиотрофическом боковом склерозе или моторной нейропатии);
– У пациентов с субклиническими или клиническими признаками нарушения нервно-мышечной передачи (например, при миастении гравис или синдроме Ламберта-Итона);
– У больных, имеющих высокий риск развития закрытоугольной глаукомы, включая анатомическое сужение угла передней камеры глаза.
– У пациентов с повышенной чувствительностью к препаратам, содержащим белки, следует учитывать риск развития аллергической реакции и до проведения процедуры оценивать возможную пользу от лечения.
Применение при беременности и в период грудного вскармливания
Беременность
Известно, что ботулинический токсин А обладает репродуктивной токсичностью у животных. Контролируемых клинических исследований репродуктивной токсичности препарата Миотокс® у человека не проводилось, поэтому применение препарата Миотокс® во время беременности и у женщин детородного возраста, не использующих надежную контрацепцию, противопоказано, за исключением случаев крайней необходимости.
Период грудного вскармливания
Неизвестно, выделяется ли ботулинический токсин А в грудное молоко, поэтому применение препарата Миотокс® в период грудного вскармливания противопоказано.
Фертильность
Известно, что ботулинический токсин А снижает фертильную способность у животных.
Контролируемых клинических исследований влияния препарата Миотокс® на фертильность человека не проводилось.
Применение препарата Миотокс® при беременности и в период грудного вскармливания противопоказано.
Способ применения и дозы
Для внутримышечного введения.
Введение препарата должно осуществляться только врачами соответствующей квалификации, которые получили специальную подготовку для проведения данного вида лечения и с использованием необходимого оборудования. Допускается проведение инъекций амбулаторно в условиях процедурного кабинета.
В начале терапии необходимо использовать минимальные рекомендуемые дозы. При последующих курсах инъекций эта доза может быть постепенно увеличена до максимально рекомендованной дозы, если это необходимо.
Универсальные оптимальные дозы и количество внутримышечных инъекций не определены для всех показаний. В таких случаях индивидуальный режим лечения для конкретного пациента должен быть определен врачом в соответствии с выраженностью и локализацией мышечной гиперактивности. Оптимальные дозы должны подбираться с помощью титрации, но рекомендуемая максимальная доза препарата не должна быть превышена. В некоторых случаях для более точного установления локализации патологического процесса используется электромиография.
Приготовление и хранение разведенного препарата
Приготовление разведенного раствора и его набор в шприц следует проводить на рабочей поверхности, покрытой бумажным полотенцем в полиэтиленовой подкладке, что дает возможность быстро удалить пролитый препарат.
Флакон препарата содержит 100 ЕД в 1,0 мл раствора. При необходимости, перед применением, для достижения желаемой концентрации, раствор препарата можно дополнительно развести 1 – 7 мл 0,9 % раствором натрия хлорида для инъекций. Флакон с препаратом помещают на рабочую поверхность и обрабатывают часть резиновой пробки этиловым спиртом. Пробку прокалывают стерильной иглой размером 23-25 G и вводят необходимое количество растворителя во флакон. Запрещается открывать флакон и удалять пробку. После вскрытия (прокалывания пробки флакона) препарат может храниться в оригинальном флаконе при температуре от 2 до 8 C не более 72 часов. После разведения препарат может быть использован в течение 24 часов при условии правильного хранения.
Неиспользованный препарат должен быть утилизирован в соответствии с действующими правилами уничтожения биологических отходов.
Препарат вводят инсулиновым или туберкулиновым шприцем. При введении препарата в мышцы лица положение пациента сидя, затылок зафиксирован.
Концентрации, получаемые при разведении препарата:
| Объем 0,9 % раствора натрия хлорида для инъекций, добавленного во флакон (мл) | Полученный объем препарата во флаконе (мл) | Полученная доза (ЕД на 0,1 мл) |
| без добавления NaCl | 1 | 10 |
| 1 | 2 | 5 |
| 1,5 | 2,5 | 4 |
| 3 | 4 | 2,5 |
| 4 | 5 | 2 |
| 7 | 8 | 1,25 |
Дозы, схемы и способы введения препарата при блефароспазме
Препарат Миотокс® следует вводить внутримышечно в дозе 1,25-2,5 ЕД в каждую точку введения. При лечении двустороннего блефароспазма препарат вводить поверхностно внутримышечно шприцом с иглой калибром 28-30 G в следующие точки: две точки на верхнем веке, 1 точка на латеральной половине нижнего века и 1 точка у латерального угла глаза. Суммарная начальная доза не должна превышать 25 ЕД с каждой стороны.
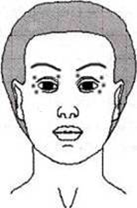
Рис. 1. Точки введения препарата Миотокс® при блефароспазме
Для профилактики возникновения птоза, как осложнения процедуры, необходимо избегать введения препарата вблизи мышцы, поднимающей верхнее веко. Для профилактики диплопии, как осложнения процедуры, необходимо избегать введения препарата в медиальную часть нижнего века.
Дозы, схемы и способы введения препарата при цервикальной дистонии (спастической кривошее)
Раствор препарата вводят иглой размером 25-30 G. В клинических исследованиях, проводившихся с целью установления безопасности и эффективности препарата при цервикальной дистонии, суммарная доза разведенного препарата составила 200 ЕД.
Как и при любом медикаментозном лечении, для пациентов, не получавших ранее терапии ботулиническим токсином, в качестве начальной дозы используется минимальная эффективная доза. Суммарная доза 200 ЕД распределяется между спастичными мышцами шеи: m. splenis capitis, m. trapesius, m. sternocleidomasoideus, m. scalenus и m. levator scapulae. Инъецируемые мышцы выбираются врачом в зависимости от типа дистонии (антеро-, ретро-, латеро- или торти-коллис) индивидуально для каждого пациента.
При сложных формах кривошеи или слабом эффекте от лечения следует провести ЭМГ мышц шеи для более точного установления локализации напряженных мышц.
Дозы, схемы и способы введения препарата при коррекции мимических морщин:
Оптимальные дозы и число точек инъекций в одну мышцу могут отличаться у разных пациентов, поэтому необходимо выбирать индивидуальный режим дозирования.
Согласно данным клинических исследований, суммарная доза препарата составляет 30-50 ЕД в зависимости от глубины морщин.
Сглаживание межбровных морщин
В процессе формирования межбровных морщин участвуют m. corrugator supercilii (мышца, сморщивающая бровь) и m. procerus (мышца гордецов).
Для определения места инъекций пациента просят нахмуриться, в этот момент хорошо пальпируются m. corrugator supercilli, при этом отмечают точку наиболее выраженной мышечной активности, которая должна находиться на 0,5 см выше верхнего медиального края брови. Аналогичным образом производят разметку на другой стороне. Отмечают точку введения препарата в m. рrocerus, которая располагается в середине линии, соединяющей медиальные края бровей.
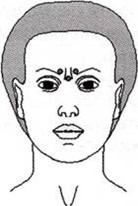
Рис. 2. Точки введения препарата Миотокс® для разглаживания морщин в межбровной области
Игла вводится в толщу брюшка, направление иглы – либо под углом 45° спереди назад, медиально, либо под углом 90°. Глубина введения иглы – 7-10 мм. Если игла упрется в надкостницу, ее надо вытянуть из тканей на 1 мм и после этого ввести препарат.
В каждую отмеченную точку вводят от 4 до 6 ЕД препарата или вводят по 4-4,5 ЕД препарата в обозначенные три точки и по 3 ЕД в две дополнительные латеральные точки m. corrugator supercilii, которые располагаются на 5-7 мм выше и латеральнее первичных. Суммарная доза веденного при коррекции морщин межбровья препарата составляет 15-20 ЕД.
Для снижения риска развития птоза необходимо избегать введения препарата вблизи мышцы, поднимающей верхнее веко, особенно у пациентов с хорошо выраженной мышцей, опускающей бровь. При введении препарата в мышцу, сморщивающую бровь, инъекции необходимо производить в центральную часть мышцы, отступив не менее чем на 1 см выше дуги брови.
Сглаживание горизонтальных морщин в области лба
В образовании горизонтальных морщин в области лба участвует m. epicranius (надчерепная мышца), а именно ее лобная порция m. frontalis.
Для сглаживания лобных морщин пациента просят поднять брови и на максимуме амплитуды отмечают точки с наиболее выраженной мимической активностью. С целью исключения птоза брови, расстояние между точкой инъекции и верхним краем брови должно составлять не менее 2 см. Отмечается от 5 до 10 точек, их количество определяется врачом индивидуально для каждого пациента. Суммарная доза препарата, введенная в лобную мышцу должна составить 10-15 ЕД. Данное количество препарата равномерно распределяется на все отмеченные точки.
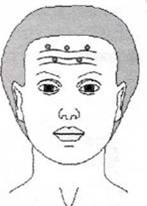
Рис. 3. Точки введения препарата Миотокс® для разглаживания морщин в области лба
При проведении процедуры следует учитывать, что выраженные инволюционные изменения кожи лба ведут к значительному увеличению риска опущения бровей, что требует снижения дозировок или отказа от введения препарата во фронтальную область. Для уменьшения риска птоза бровей инъекции должны осуществляться на расстоянии не менее 2-3 см от края брови.
Сглаживание морщин в периорбитальной области
Морщины, расходящиеся радиально вокруг глаз, так называемые «гусиные лапки», возникают в результате активности круговой мышцы глаза. Для выбора точек введения и дозы препарата пациента просят прищуриться и/или улыбнуться и в это время очерчивают примерные границы области с максимальным количеством складок.
Для коррекции «гусиных лапок» инъекции препарата проводят в проекции m. orbicularis oculi (круговая мышца глаза) в 2-4 точки с каждой стороны в область латеральной части нижнего века в местах максимальной мышечной активности. Точки должны располагаться на расстоянии не менее чем 1 см от наружного угла глаза в местах максимальной мышечной активности.
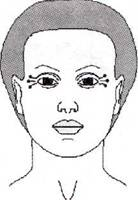
Рис. 4. Точки введения препарата Миотокс® для разглаживания морщин в периорбитальной области
B каждую точку вводят 1 - 3 ЕД препарата, так чтобы суммарная доза препарата с каждой стороны составила 2,5-7,5 ЕД. Максимальная доза не должна превышать 20 ЕД препарата с каждой стороны за одну процедуру. Чтобы не нарушать пропорций лица необходимо тщательно следить за симметричностью расположения точек введения. Препарат в области «гусиных лапок» не вводится очень низко и глубоко, так как возможно нарушение симметричности углов рта и носогубной складки вследствие диффузии препарата в область m. zygomatius major (большая скуловая мышца).
Дозы, схемы и способы введения препарата при лечении фокальной спастичности у детей с детским церебральным параличом:
Раствор препарата Миотокс® вводят иглой размером 23-26G / 0,60-0,45 мм.
При лечении фокальной спастичности, ассоциированной с динамической деформацией стопы по типу «конская стопа» вследствие спастичности у детей с детским церебральным параличом, препарат вводят в две точки каждой головки икроножной мышцы (медиальной и латеральной). При поражении одной конечности доза составляет 4 ЕД/кг массы тела. При диплегии общая доза составляет - 6 ЕД/кг массы тела на обе пораженные конечности. Общая доза не должна превышать 200 ЕД.
Клиническое улучшение проявляется в первые 7-14 дней после инъекции. Препарат вводят повторно при снижении выраженности клинического эффекта наполовину, но не ранее, чем через 3 месяца после предшествующей процедуры. Дозу препарата подбирают таким образом, чтобы добиться как минимум 6-месячного интервала между процедурами. Улучшению клинического эффекта от инъекций препарата Миотокс® могут способствовать ортопедическая коррекция, растяжение мышц и физиотерапия.
Общие рекомендации для всех показаний к применению
При неэффективности первой процедуры, по сравнению с исходным состоянием, при любом выше описанном лечении, через 1 месяц после введения препарата, необходимо:
1. Клиническое подтверждение действия токсина на инъецированную мышцу (мышцы), которое может включать электромиографическое (ЭМГ) исследование, выполняемое опытным специалистом в специализированном отделении;
2. Анализ причин неэффективности процедуры, например, неадекватный выбор точек для инъекции, недостаточная доза, неправильная техника инъекции, признаки фиксированной контрактуры, слабость мышц-антагонистов, формирование токсиннейтрализующих антител;
3. Повторная оценка целесообразности лечения ботулиническим токсином типа А;
4. При отсутствии каких-либо нежелательных эффектов, связанных с первым введением препарата, при повторной процедуре должны быть соблюдены следующие условия: коррекция дозы с учетом анализа причин неэффективности предыдущей процедуры; ЭМГ – контроль; интервал между процедурами должен составлять не менее 3 мес.
5. При отсутствии эффекта от введения препарата или снижения его выраженности после повторных инъекций, следует рекомендовать другие методы лечения.
Особые группы пациентов
Пожилые пациенты
Адекватных исследований дозировок в гериатрической популяции не проводилось. Рекомендовано использование наименьшей дозы, необходимой для достижения эффекта, соблюдая наибольший клинически допустимый интервал между введениями. При лечении пожилых пациентов с отягощенным анамнезом и сопутствующей терапией необходимо соблюдать осторожность.
Побочное действие
Указанные побочные эффекты и нежелательные реакции выявлены в ходе клинических исследований, а также в ходе опыта применения препаратов, содержащих ботулинический токсин типа А в качестве действующего вещества.
Как правило, нежелательные реакции проявляются в течение первых дней после инъекции и являются преходящими. В редких случаях длительность нежелательных реакций может составлять несколько месяцев и более.
Локальная мышечная слабость отражает ожидаемое фармакологическое действие ботулинического токсина на мышцу. Однако большие дозы могут вызвать слабость мышц помимо непосредственно тех, что локализованы в месте инъекций.
Как и при любой инъекционной процедуре, в месте введения могут отмечаться локальная болезненность, воспаление, парестезии, гипестезии, уплотнение кожи, отечность, эритема, локализованная инфекция, кровотечение и / или гематомы. Связанная с процедурой боль и / или тревога могут приводить к вазовагальным реакциям, включая транзиторную гипотензию и обмороки.
Описано повышение температуры и возникновение гриппоподобного синдрома.
Указанные ниже побочные эффекты приведены в соответствии с частотой их возникновения и представлены для каждого показания: очень часто (≥1/10), часто (<1/10, ≥ 1/100), нечасто (<1/100, ≥ 1/1000), редко (<1/1000, ≥ 1/10 000), очень редко (<1/10 000).
Блефароспазм
Нарушения со стороны нервной системы:
Нечасто: головокруж

